 Thu hồi toàn quốc một lô sản phẩm Gel AG Nano TP Plus do vi phạm chất lượng vi sinh.
Thu hồi toàn quốc một lô sản phẩm Gel AG Nano TP Plus do vi phạm chất lượng vi sinh.
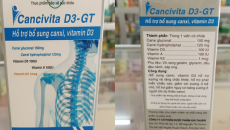
Thu hồi 2 lô thực phẩm bảo vệ sức khỏe Cancivita D3-GT
Thu hồi hàng loạt mỹ phẩm vi phạm về nhãn và công thức
Thêm một lô sữa rửa mặt Gammaphil kém chất lượng bị thu hồi
Thu hồi kem massage có công thức không đúng như hồ sơ đã công bố
Cụ thể, lô sản phẩm Gel AG Nano TP Plus - Hộp 1 tuýp 20g. Trên nhãn ghi: Số tiếp nhận Phiếu công bố: 06/23/CBMP-HY; Số lô: 072024; NSX: 16/7/2024; HSD: 15/7/2027; Tổ chức chịu trách nhiệm đưa sản phẩm ra thị trường: Công ty cổ phần xuất nhập khẩu TH Pharma (Địa chỉ: Số 10 dãy X1, ngõ 11, đường Tô Hiệu, phường Nguyễn Trãi, quận Hà Đông, TP. Hà Nội), Công ty TNHH dược mỹ phẩm Quang Xanh (Địa chỉ: Thôn Hành Lạc, thị trấn Như Quỳnh, huyện Văn Lâm, tỉnh Hưng Yên) sản xuất.
Trước đó, Trung tâm Kiểm nghiệm thuốc, mỹ phẩm, thực phẩm - Sở Y tế tỉnh Nghệ An đã lấy mẫu mỹ phẩm trên tại Nhà thuốc 365 trên địa bàn tỉnh để kiểm tra chất lượng. Tuy nhiên, mẫu thử không đạt tiêu chuẩn chất lượng về chỉ tiêu giới hạn vi sinh vật, đây cũng chính là lý do khiến Cục Quản lý Dược quyết định thu hồi.
Trên các website bán hàng, sản phẩm Gel AG Nano TP Plus được mô tả có công dụng giúp làm sạch da, giúp dưỡng ẩm, làm dịu da, giúp kháng khuẩn và giúp phòng ngừa các tác nhân gây: nấm, ngứa, viêm da, lở loét,...
Cục Quản lý Dược đề nghị Sở Y tế các tỉnh, thành phố trực thuộc Trung ương thông báo cho các cơ sở kinh doanh và sử dụng mỹ phẩm trên địa bàn ngừng ngay việc kinh doanh, sử dụng lô sản phẩm Gel AG Nano TP Plus nêu trên và trả lại cho cơ sở cung ứng sản phẩm. Các Sở Y tế cũng được yêu cầu tiến hành thu hồi và tiêu hủy lô sản phẩm vi phạm; đồng thời kiểm tra, giám sát các đơn vị thực hiện thông báo này và xử lý các vi phạm theo quy định hiện hành.
Về phía Công ty Cổ phần Xuất Nhập khẩu TH Pharma và Công ty TNHH Dược Mỹ phẩm Quang Xanh, cả hai đơn vị phải gửi thông báo thu hồi tới những nơi phân phối, sử dụng lô sản phẩm Gel AG Nano TP Plus. Các công ty này có trách nhiệm tiếp nhận sản phẩm trả lại từ các cơ sở kinh doanh và tiến hành thu hồi, tiêu hủy toàn bộ lô sản phẩm không đạt chuẩn. Báo cáo thu hồi và tiêu hủy lô sản phẩm phải được gửi về Cục Quản lý Dược trước ngày 21/8/2025.
Đặc biệt, Cục Quản lý Dược cũng đề nghị Sở Y tế TP. Hà Nội và Sở Y tế tỉnh Hưng Yên giám sát Công ty cổ phần xuất nhập khẩu TH Pharma và Công ty TNHH dược mỹ phẩm Quang Xanh trong việc thực hiện thu hồi và tiêu hủy lô sản phẩm Gel AG Nano TP Plus. Hai Sở Y tế này cũng cần kiểm tra các công ty về việc chấp hành các quy định của pháp luật về quản lý mỹ phẩm, xử lý các vi phạm và báo cáo kết quả kiểm tra, giám sát về Cục Quản lý Dược trước ngày 5/9/2025.
Trước đó, vào ngày 30/7, Cục Quản lý Dược cũng ban hành quyết định ngừng tiếp nhận hồ sơ đề nghị cấp, gia hạn giấy đăng ký lưu hành thuốc, nguyên liệu làm thuốc với Công ty Cổ phần Dược phẩm MeDiSun (521 Khu phố An Lợi, Phường Hòa Lợi, TP Hồ Chí Minh (Địa chỉ cũ: 521 Khu phố An Lợi, Phường Hòa Lợi, Thị xã Bến Cát, tỉnh Bình Dương), do sản xuất 2 lô thuốc vi phạm chất lượng.
Theo quy định của Luật Dược, một doanh nghiệp sẽ bị thu hồi giấy đăng ký lưu hành thuốc nếu có ít nhất hai lô sản phẩm bị thu hồi bắt buộc do vi phạm mức độ 2 trong vòng 5 năm kể từ ngày cấp phép. Vi phạm chất lượng mức độ 2 được định nghĩa là thuốc không đạt tiêu chuẩn ở các chỉ tiêu không định tính, không trực tiếp đe dọa nghiêm trọng đến sức khỏe hay tính mạng người dùng, nhưng có thể ảnh hưởng đến hiệu quả điều trị hoặc tiềm ẩn rủi ro khi sử dụng lâu dài, liều cao.
Sau khi thời hạn 12 tháng ngừng tiếp nhận hồ sơ kết thúc, Công ty Cổ phần Dược phẩm MeDiSun sẽ phải nộp lại hồ sơ theo đúng quy định nếu muốn tiếp tục đăng ký thuốc hoặc nguyên liệu làm thuốc.


























Bình luận của bạn