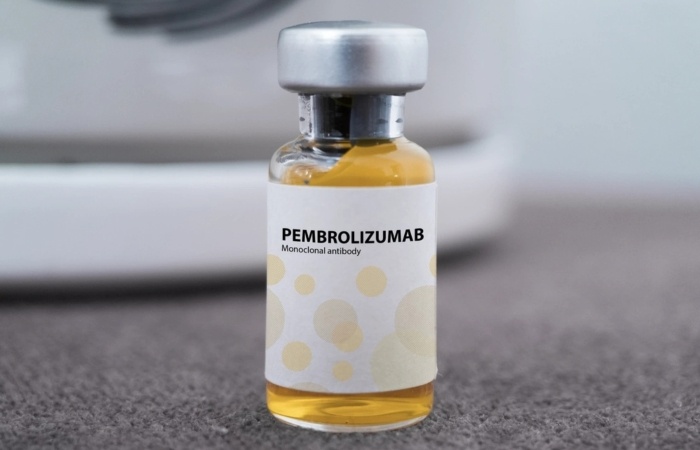
 Thuốc chống ung thư Pembroria có hoạt chất chính là Pembrolizumab do Nga sản xuất - Ảnh: incentra.
Thuốc chống ung thư Pembroria có hoạt chất chính là Pembrolizumab do Nga sản xuất - Ảnh: incentra.
Mỹ thu hồi nửa triệu chai thuốc huyết áp do chứa tạp chất gây ung thư
Ngày càng nhiều người trẻ mắc ung thư đại tràng, làm sao để phòng ngừa?
AstraZeneca đẩy mạnh hợp tác trong chẩn đoán và điều trị ung thư vú tại Việt Nam
Đột phá: Xét nghiệm máu mới giúp phát hiện sớm hơn 50 loại ung thư
Theo Quyết định số 628/QĐ-QLD ngày 31/10/2025 của Cục Quản lý Dược, Pembroria nằm trong danh mục 14 vaccine và sinh phẩm được cấp phép lưu hành tại Việt Nam đợt 57, có hiệu lực trong 3 năm. Thuốc do Công ty Limited Liability “PK-137” (Nga) sản xuất, được Anabion Pharmaceutical Trading Ltd (Các Tiểu Vương quốc Ả Rập Thống nhất) đứng tên đăng ký.
Pembroria chứa hoạt chất Pembrolizumab (100mg/4ml) – một kháng thể đơn dòng thuộc nhóm ức chế điểm kiểm soát miễn dịch PD-1, có tác dụng giúp hệ miễn dịch nhận diện và tiêu diệt tế bào ung thư. Thuốc được bào chế dưới dạng dung dịch đậm đặc pha tiêm truyền, có hạn sử dụng 24 tháng kể từ ngày sản xuất.
Theo thông tin từ cơ sở đăng ký, Pembrolizumab có hơn 14 chỉ định cho các loại bệnh ung thư khác nhau (như ung thư biểu mô phổi, u hắc tố, ung thư đại trực tràng, ung thư cổ tử cung, ung thư biểu mô tế bào thận, ung thư vú...).
Cục Quản lý Dược yêu cầu sau khi được cấp giấy đăng ký lưu hành, công ty phải định kỳ 03 tháng một lần kể từ ngày cấp giấy đăng ký lưu hành thực hiện cập nhật tiến độ triển khai nghiên cứu lâm sàng theo dõi tính sinh miễn dịch pha III (giai đoạn thử nghiệm được nghiên cứu trên quy mô lớn nhằm xác định tính ổn định của công thức, tính an toàn, hiệu quả điều trị ở mức tổng thể của thuốc hoặc để đánh giá hiệu quả bảo vệ và tính an toàn của vắc xin trên đối tượng đích) và nộp hồ sơ thay đổi, bổ sung cập nhật dữ liệu theo dõi tính sinh miễn dịch pha III khi thời gian nghiên cứu kết thúc.
Được biết, hoạt chất Pembrolizumab trong thuốc Pembroria cũng chính là thành phần của thuốc điều trị ung thư Keytruda, do hãng Merck Sharp & Dohme (Mỹ) sản xuất, đã được Bộ Y tế Việt Nam cấp phép lưu hành từ năm 2017.
Do đó, thuốc ung thư của Nga mới được cấp đăng ký không phải là thuốc mới, mà là thuốc sinh học tương tự (Biosimilars) của thuốc gốc Keytruda. Đây là loại thuốc được phát triển khi thuốc gốc hết thời hạn bảo hộ sở hữu trí tuệ, có hiệu quả và độ an toàn tương đương, nhưng giá thành thấp hơn, giúp tăng khả năng tiếp cận điều trị cho bệnh nhân ung thư.
Việc cấp phép này là một bước quan trọng trong chiến lược mở rộng tiếp cận thuốc, vaccine và sinh phẩm chất lượng cao cho người dân Việt Nam, đồng thời góp phần đảm bảo an ninh y tế, đa dạng hóa nguồn cung thuốc và vaccine trong bối cảnh nhu cầu phòng bệnh và điều trị ngày càng tăng.
Thông tin thêm về Pembrolizumab
Pembrolizumab, được biết đến nhiều dưới tên biệt dược Keytruda, là thuốc điều trị ung thư theo cơ chế miễn dịch. Thuốc hoạt động bằng cách ngăn protein PD-1 trên tế bào T (một loại bạch cầu thuộc dòng tế bào lympho, đóng vai trò quan trọng trong hệ thống miễn dịch đáp ứng của cơ thể) gắn với PD-L1 hoặc PD-L2 trên tế bào ung thư, giúp khôi phục hoạt động của hệ miễn dịch để tiêu diệt tế bào ác tính.
Các chỉ định chính của Pembrolizumab gồm:
- Ung thư phổi không tế bào nhỏ (NSCLC) giai đoạn tiến triển.
- U hắc tố (melanoma) ác tính.
- Ung thư biểu mô tế bào vảy đầu cổ, cổ tử cung, dạ dày – thực quản, gan, thận.
- U lympho Hodgkin kinh điển và một số loại ung thư có biểu hiện PD-L1 cao.
Tác dụng phụ có thể gặp là phát ban, mệt mỏi, đau khớp, viêm phổi, rối loạn tuyến giáp, và các phản ứng miễn dịch khác. Bệnh nhân được khuyến cáo không tự ý sử dụng thuốc, cần có chỉ định và theo dõi nghiêm ngặt của bác sĩ chuyên khoa ung thư.

























Bình luận của bạn